Cientistas do MIT despojam o câncer de sua armadura de açúcar
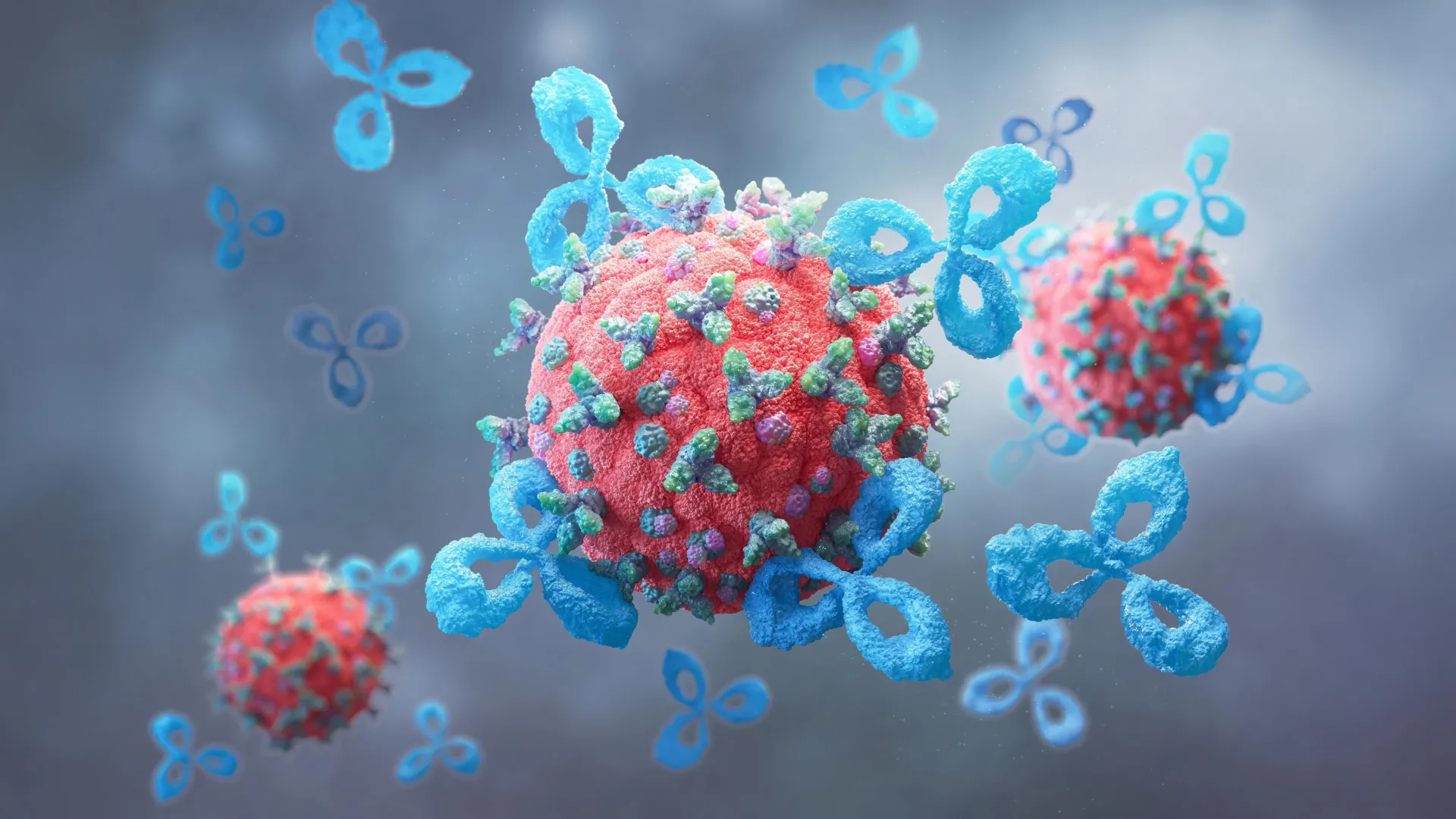
Uma equipe de pesquisa do MIT e da Universidade de Stanford desenvolveu uma nova técnica projetada para estimular o sistema imunológico a atacar células tumorais. A estratégia tem como objetivo ajudar a imunoterapia do câncer a ser bem-sucedida em um número muito maior de pacientes do que é atualmente.
No centro desse trabalho está um método para reverter um “freio” natural que os tumores podem ativar para impedir a agressão das células imunológicas. Esse freio está relacionado a açúcares chamados glicanos, que se encontram na superfície das células cancerosas.
Os cientistas descobriram que bloquear esses glicanos com proteínas conhecidas como lectinas pode fortalecer consideravelmente a atividade imunológica contra as células cancerosas. Para fazer isso de maneira direcionada, eles construíram moléculas multifuncionais chamadas AbLecs, que combinam uma lectina com um anticorpo que se fixa nos tumores.
“Criamos um novo tipo de terapia proteica que pode bloquear os pontos de controle imunológicos baseados em glicanos e aumentar as respostas imunológicas contra o câncer”, afirma Jessica Stark, professora da Carreira Underwood-Prescott nos departamentos de Engenharia Biológica e Engenharia Química. “Como os glicanos são conhecidos por restringir a resposta imunológica ao câncer em vários tipos de tumores, suspeitamos que nossas moléculas possam oferecer novas e potencialmente mais eficazes opções de tratamento para muitos pacientes com câncer.”
Stark, que também é membro do Instituto Koch de Pesquisa Integrativa do Câncer do MIT, liderou o estudo como autora principal do artigo. Carolyn Bertozzi, professora de química em Stanford e diretora do Sarafan ChEM Institute, atuou como autora sênior. Os resultados foram publicados na Nature Biotechnology.
Como o Câncer Usa os Freios Imunológicos
Um dos principais objetivos no tratamento do câncer é ensinar o sistema imunológico a reconhecer e eliminar células tumorais. Um grupo importante de medicamentos de imunoterapia chamados inibidores de ponto de checagem atua interrompendo a interação entre duas proteínas, PD-1 e PD-L1. Ao bloquear essa conexão, esses medicamentos removem um freio que os tumores utilizam para impedir que células imunológicas, como as células T, matem as células cancerosas.
Inibidores de ponto de checagem que visam a via PD-1 PD-L1 já foram aprovados para vários tipos de câncer. Para algumas pessoas, eles podem resultar em remissão duradoura. No entanto, para muitos outros, oferecem pouco ou nenhum benefício.
Devido a essa lacuna, os pesquisadores estão em busca de outras maneiras pelas quais os tumores suprimem o sistema imunológico. Um alvo promissor envolve as interações entre glicanos tumorais e receptores em células imunológicas.
Siglecs, Ácido Sialico e um Ponto de Checagem Baseado em Açúcar
Glicanos aparecem em quase todas as células vivas, mas células cancerosas costumam apresentar versões que não são encontradas em células saudáveis. Muitos desses glicanos específicos de tumor incluem uma unidade de construção de açúcar chamada ácido sialico. Quando ácidos sialicos se ligam a receptores de lectina em células imunológicas, eles podem ativar uma via de atenuação imunológica. As lectinas que reconhecem o ácido sialico são chamadas de Siglecs.
“Quando Siglecs em células imunológicas se ligam aos ácidos sialicos em células cancerosas, isso reduz a resposta imunológica. Impede que essa célula imunológica seja ativada para atacar e destruir a célula cancerosa, assim como acontece quando PD-1 se liga a PD-L1,” diz Stark.
Até o momento, não existem medicamentos aprovados que visem diretamente a interação entre Siglec e ácido sialico, embora muitas abordagens tenham sido exploradas. Uma ideia tem sido criar lectinas que se liguem aos ácidos sialicos e bloqueiem seu contato com células imunológicas. No entanto, isso tem enfrentado dificuldades porque as lectinas normalmente não se ligam com força suficiente para se acumular em grandes quantidades na superfície das células cancerosas.
AbLecs Combinam Anticorpos e Lectinas
Para solucionar esse problema, Stark e sua equipe utilizaram anticorpos como veículos de entrega para levar mais lectinas aos tumores. A parte do anticorpo direciona células cancerosas e, assim que chega, a lectina anexada pode se ligar ao ácido sialico. Isso bloqueia o ácido sialico de interagir com os receptores Siglec em células imunológicas, removendo o freio imunológico e permitindo que células imunológicas, como macrófagos e células NK (natural killer), ataquem o tumor.
“Esse domínio de ligação da lectina normalmente tem uma afinidade relativamente baixa, então não pode ser utilizado sozinho como um terapêutico. Mas, quando o domínio de lectina está ligado a um anticorpo de alta afinidade, é possível chegar à superfície da célula cancerosa, onde pode se ligar e bloquear os ácidos sialicos,” explica Stark.
Um Design Modular Testado em Células e Camundongos
Para este estudo, os pesquisadores desenvolveram um AbLec utilizando trastuzumabe, um anticorpo que se liga ao HER2 e é aprovado para o tratamento de câncer de mama, estômago e colorretal. Para criar o AbLec, eles substituíram um dos braços do anticorpo por uma lectina, escolhendo entre Siglec-7 ou Siglec-9.
Em experimentos laboratoriais com células cultivadas, este AbLec alterou o comportamento das células imunológicas, incentivando-as a atacar e eliminar as células cancerosas.
A equipe também testou os AbLecs em camundongos geneticamente modificados para expressar receptores humanos de Siglec e receptores de anticorpos humanos. Após a introdução de células cancerosas que formaram metástases pulmonares, o tratamento com o AbLec resultou em menos metástases pulmonares do que o tratamento apenas com trastuzumabe.
Os pesquisadores também demonstraram que a abordagem é flexível. Eles podiam trocar diferentes anticorpos que visam tumores, como rituximabe, que mira o CD20, ou cetuximabe, que tem como alvo o EGFR. Além disso, podiam alterar a parte da lectina para atingir outros glicanos imunossupressores ou utilizar anticorpos que visam proteínas de ponto de checagem, como PD-1.
“Os AbLecs são realmente plug-and-play. Eles são modulares,” diz Stark. “Você pode imaginar a troca de diferentes domínios de receptor decoy para direcionar diferentes membros da família de receptores de lectina, além de trocar o braço do anticorpo. Isso é importante porque diferentes tipos de câncer expressam diferentes antígenos, que você pode abordar alterando o alvo do anticorpo.”
Próximos Passos e Financiamento
Stark, Bertozzi e colegas fundaram uma empresa chamada Valora Therapeutics para desenvolver candidatos principais de AbLec. Eles pretendem iniciar ensaios clínicos nos próximos dois a três anos.
O financiamento para o trabalho foi parcialmente obtido por meio de um Prêmio de Carreira do Burroughs Wellcome Fund na Interface Científica, um Prêmio Steven A. Rosenberg da Sociedade para Imunoterapia do Câncer, uma Bolsista V da V Foundation, do Instituto Nacional do Câncer, do Instituto Nacional de Ciências Médicas Gerais, uma bolsa de descoberta biológica da Merck, uma Bolsa de Pós-Doutorado da Sociedade Americana do Câncer e uma bolsa inicial de Sarafan ChEM-H para Pós-Doutores na Interface.