Imported Article – 2026-02-09 07:00:19
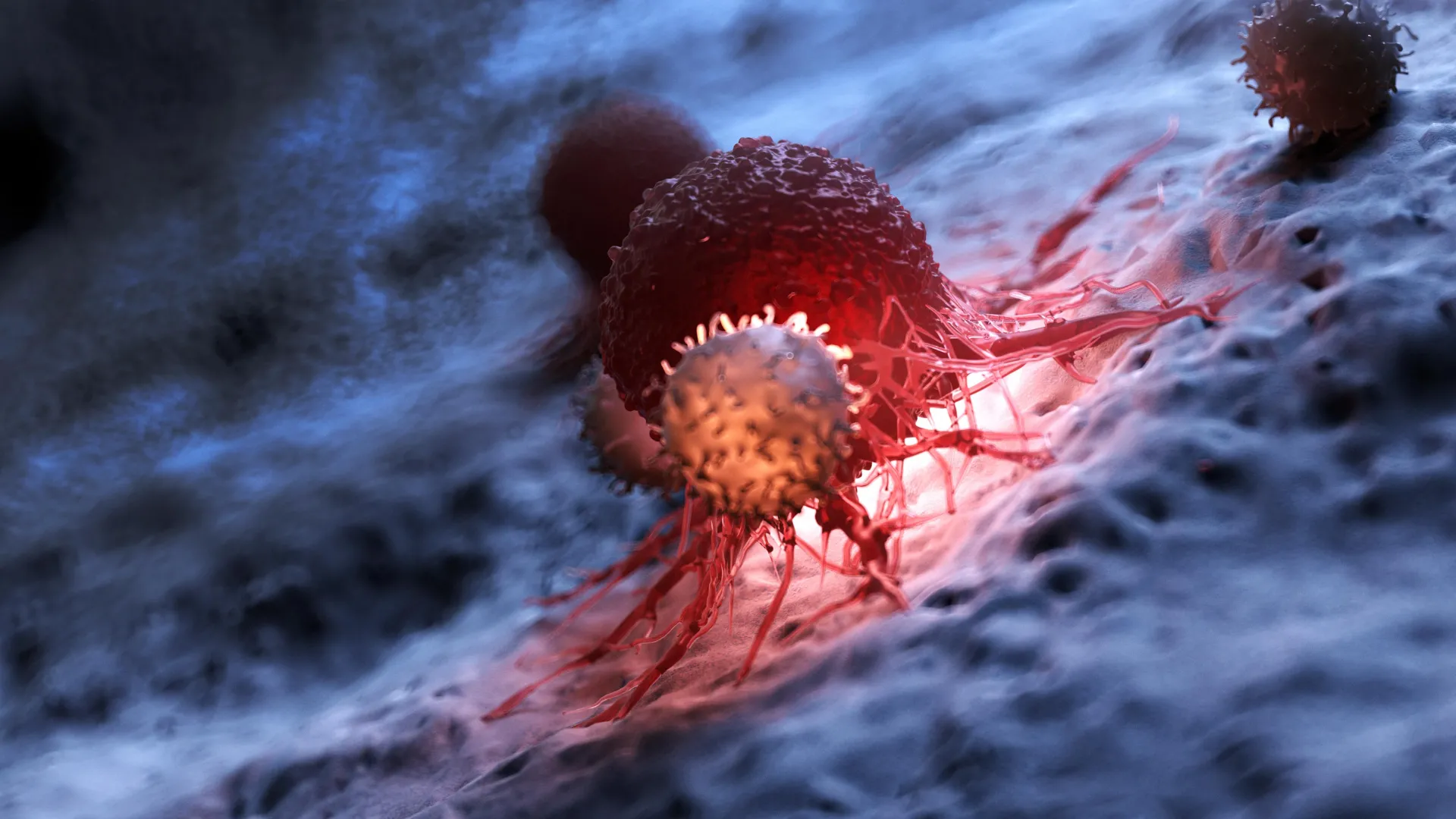
A imunoterapia contra o câncer transformou o tratamento oncológico ao treinar o sistema imunológico do corpo para reconhecer e atacar tumors. Medicamentos conhecidos como inibidores de checkpoint imunológico, que visam a via PD-1/PD-L1, resultaram em respostas duradouras em alguns pacientes, aumentando a esperança em relação ao controle prolongado do câncer. No entanto, para a maioria das pessoas, essas terapias não oferecem os mesmos benefícios. Os tumores conseguem se adaptar e desenvolver maneiras de escapar da detecção imunológica, limitando a eficácia do tratamento.
Esse desafio levou os pesquisadores a explorar além do próprio tumor e examinar mecanismos mais amplos de resistência imunológica. Os cientistas estão se concentrando cada vez mais em como os cânceres suprimem a atividade do sistema imunológico em todo o corpo, e não apenas no local do tumor. Uma área emergente de interesse envolve vesículas extracelulares pequenas (sEVs), partículas minúsculas liberadas por células cancerígenas que podem carregar moléculas imunossupressoras e enfraquecer a resposta imunológica de maneiras que ainda não são totalmente compreendidas.
Investigando como o PD-L1 é Embalado e Liberado
Para entender melhor esse processo, uma equipe de pesquisa da Universidade de Saúde Fujita no Japão, liderada pelo Professor Kunihiro Tsuchida, colaborou com pesquisadores do Hospital da Universidade Médica de Tóquio e da Universidade Médica de Tóquio. O objetivo foi descobrir como o PD-L1, uma proteína chave de checkpoint imunológico, é carregado seletivamente em sEVs e se esse caminho poderia ser alvo de terapias.
O estudo, publicado na Scientific Reports, foi construído em torno de uma pergunta central não respondida. “Células cancerígenas liberam vesículas extracelulares pequenas contendo PD-L1, que se acredita reduzir a eficácia da imunoterapia contra o câncer. No entanto, como o PD-L1 é classificado nesses vesículas ainda não estava claro.” Abordar esse mistério se tornou a base da pesquisa.
Um Novo Jogador Molecular na Resistência Imunológica
Usando uma ampla gama de técnicas, incluindo biologia molecular e celular, testes bioquímicos e farmacológicos, amostras derivadas de pacientes e bioinformática, os pesquisadores identificaram a ubiquitina-like 3 (UBL3) como um fator crucial que controla como o PD-L1 é direcionado para sEVs.
Descobriram que o PD-L1 passa por uma modificação pós-traducional previamente desconhecida envolvendo a UBL3. Essa modificação ocorre através de uma ligação dissulfeto e difere do processo clássico de ubiquitinação. Experimentos adicionais mostraram que um aminoácido específico, a cisteína 272 na região citoplasmática do PD-L1, é essencial para essa modificação.
Quando os níveis de UBL3 foram aumentados nas células cancerígenas, a quantidade de PD-L1 embalada em sEVs aumentou consideravelmente, embora o total de PD-L1 dentro das células permanecesse inalterado. Em contraste, a redução dos níveis de UBL3 resultou em uma queda clara na quantidade de PD-L1 sendo carregada para os vesículas e liberada fora da célula. Juntos, esses resultados confirmaram que a UBL3 desempenha um papel central na direção do PD-L1 para sEVs.
Estatinas Interferem em uma Via Chave de Escape Imune
Uma das descobertas mais impressionantes surgiu quando a equipe examinou medicamentos que poderiam interferir nesse processo. Descobriu-se que as estatinas, amplamente prescritas para reduzir o colesterol, bloqueiam fortemente a modificação da UBL3. Todas as estatinas clinicamente utilizadas testadas no estudo reduziram a atividade da UBL3, diminuíram a modificação do PD-L1 e diminuíram acentuadamente a quantidade de PD-L1 classificada para sEVs.
Esses efeitos ocorreram em concentrações muito baixas de medicamentos que são alcançáveis em pacientes e não estiveram associados a efeitos tóxicos nas células. Importante, amostras de sangue de pessoas com câncer de pulmão de não pequenas células mostraram um padrão semelhante. Entre os pacientes com alta expressão de PD-L1 tumoral, aqueles que tomavam estatinas apresentaram níveis significativamente mais baixos de sEVs contendo PD-L1 em seu sangue em comparação com pacientes que não usavam estatinas.
Uma análise bioinformática adicional revelou que a expressão combinada de UBL3 e PD-L1 estava associada a desfechos de sobrevivência em pacientes com câncer de pulmão. Esta descoberta destaca a potencial importância clínica desse caminho regulatório recém-identificado.
O Que Isso Significa para o Tratamento do Câncer
Em conjunto, esses resultados ajudam a explicar por que os inibidores de checkpoint imunológico frequentemente falham e sugerem uma maneira prática de melhorar seu desempenho. O estudo revela um mecanismo oculto pelo qual células cancerígenas espalham o PD-L1 imunossupressor por meio de vesículas extracelulares, permitindo que os tumores enfraqueçam as respostas imunológicas muito além de seu ambiente imediato.
Vincular esse caminho às estatinas é especialmente importante, pois esses medicamentos são amplamente utilizados, baratos e geralmente seguros. Isso levanta a possibilidade de que os achados possam ser traduzidos para a prática clínica relativamente rapidamente. Como os pesquisadores notam, “A longo prazo, essa pesquisa pode levar a imunoterapias contra o câncer mais eficazes e acessíveis. Poderia ajudar mais pacientes a se beneficiarem de tratamentos com inibidores de checkpoint imunológico, melhorando a sobrevivência e a qualidade de vida em cenários do mundo real.”
Um Novo Alvo para Superar a Resistência à Imunoterapia
Em resumo, o estudo demonstra que a modificação induzida por UBL3 promove o empacotamento de PD-L1 em sEVs e que as estatinas podem interromper esse processo, reduzindo os níveis de PD-L1 imunossupressor circulante. Ao identificar a triagem de PD-L1 associada a vesículas como um impulsionador modificável da fuga imunológica, a pesquisa abre um novo caminho promissor para enfrentar a resistência à imunoterapia contra o câncer. Adicionar estatinas às estratégias de tratamento em combinação poderia oferecer uma maneira simples e escalável de melhorar os resultados para pacientes que recebem inibidores de checkpoint imunológico.